Vol. 13 - Num. 49
Colaboraciones especiales
Displasia evolutiva de cadera: controversia sobre el cribado ecográfico universal
Manuel Paz Loveraa, Lucía Llorente Otonesb, I Rivero Callec, L Lesmes Moltóa, MR Rodríguez Díaza, M.ª José Rivero Martínd
aServicio de Pediatría. Hospital de Fuenlabrada. Fuenlabrada. Madrid. España.
bDepartamento de Pediatría. Hospital de Fuenlabrada. Madrid. España.
cHospital Clínico Universitario Santiago de Compostela. A Coruña. España.
dServicio de Pediatría. Hospital de Fuenlabrada. Universidad Rey Juan Carlos (URJ). Fuenlabrada. Madrid. España.
Correspondencia: M Paz. Correo electrónico: doc_paz@yahoo.com
Cómo citar este artículo: Paz Lovera M, Llorente Otones L, Rivero Calle I, Lesmes Moltó L, Rodríguez Díaz MR, Rivero Martín MJ. Displasia evolutiva de cadera: controversia sobre el cribado ecográfico universal. Rev Pediatr Aten Primaria. 2011;13:127-34.
Publicado en Internet: 06-04-2011 - Número de visitas: 28094
Resumen
Pese a la elevada incidencia de displasia de cadera clínicamente importante (3-5 casos por cada 1000 recién nacidos vivos) y a los ampliamente estudiados factores de riesgo principales (parto de presentación podálica, sexo femenino y antecedentes familiares de displasia evolutiva de cadera), no se ha conseguido encontrar una estrategia efectiva que reduzca la incidencia de casos tardíos. Reabrimos, a propósito de un caso, la controversia existente acerca del cribado ecográfico universal en la patología osteomuscular más frecuente de la infancia.
Palabras clave
● Cribado ● Displasia de cadera ● EcografíaIntroducción
La displasia evolutiva de cadera es la patología osteomuscular más frecuente en niños menores de dos años1. Las consecuencias de la detección tardía pueden ser significativas y se cuenta con los medios para diagnosticarla precozmente; sin embargo, sigue habiendo niños con diagnósticos tardíos y, por ende, con peores resultados funcionales2. El caso que presentamos nos ayuda a tener una perspectiva diferente en el aún no resuelto debate sobre la necesidad y conveniencia de una política de cribado universal de esta patología.
Caso clínico
Niña de 18 meses, sin antecedentes personales ni familiares de interés, cuya madre refiere que desde que comenzó a caminar, hace apenas unos días, lo hace con una visible cojera.
La exploración revelaba una niña de aspecto saludable, bien nutrida, sonriente. Los hallazgos anormales se limitaban al examen ortopédico: asimetría de pliegues inguinales y glúteos, acortamiento del miembro inferior izquierdo de 1,5 cm, discreta limitación a la abducción de cadera izquierda, no dolorosa, e hiperlordosis lumbar. A su vez, destacó un patrón de marcha anormal, oscilante, “de pato”, de Trendelemburg. La radiografía de pelvis mostró un acetábulo displásico y cadera izquierda luxada (figuras 1 y 2).
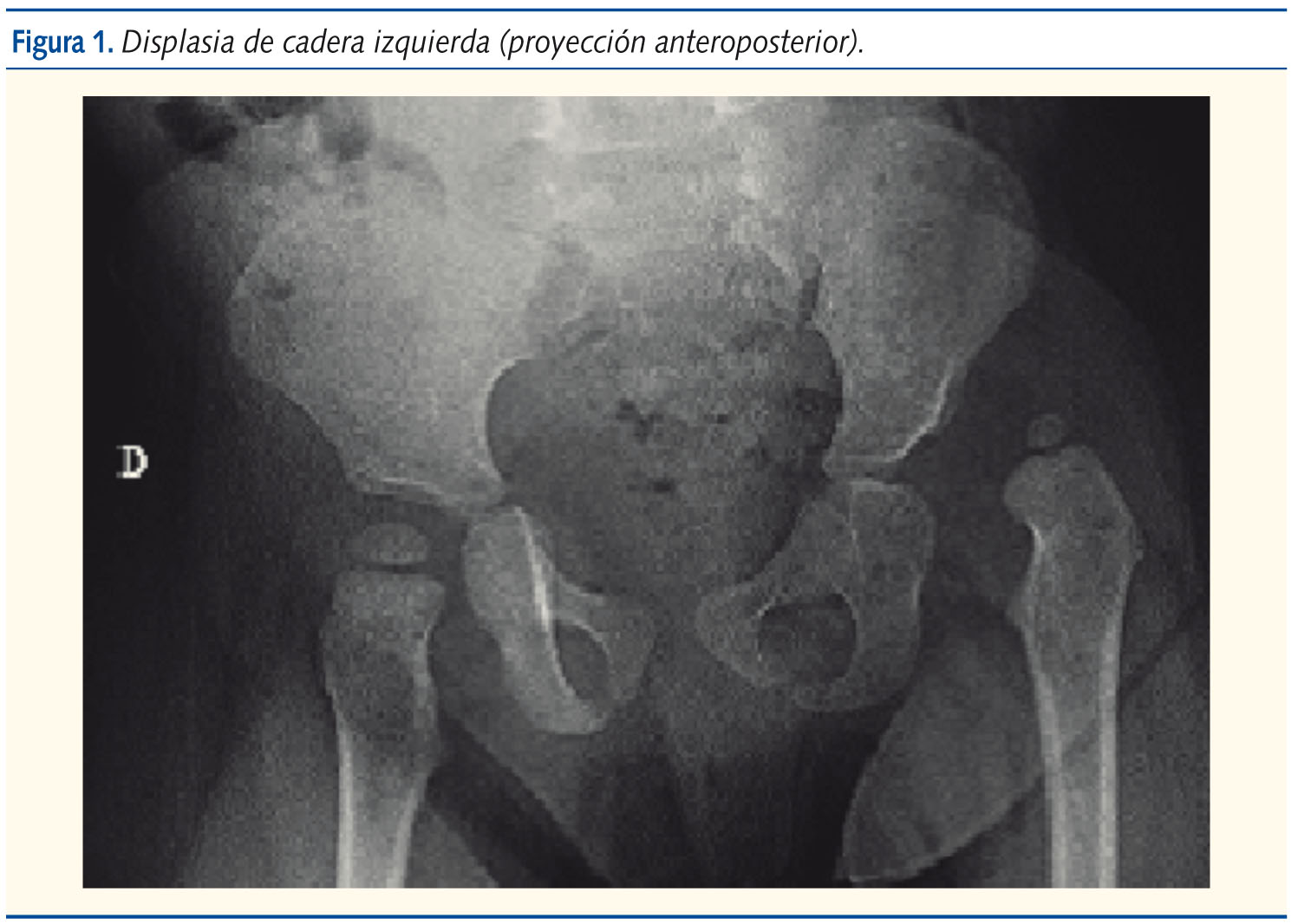
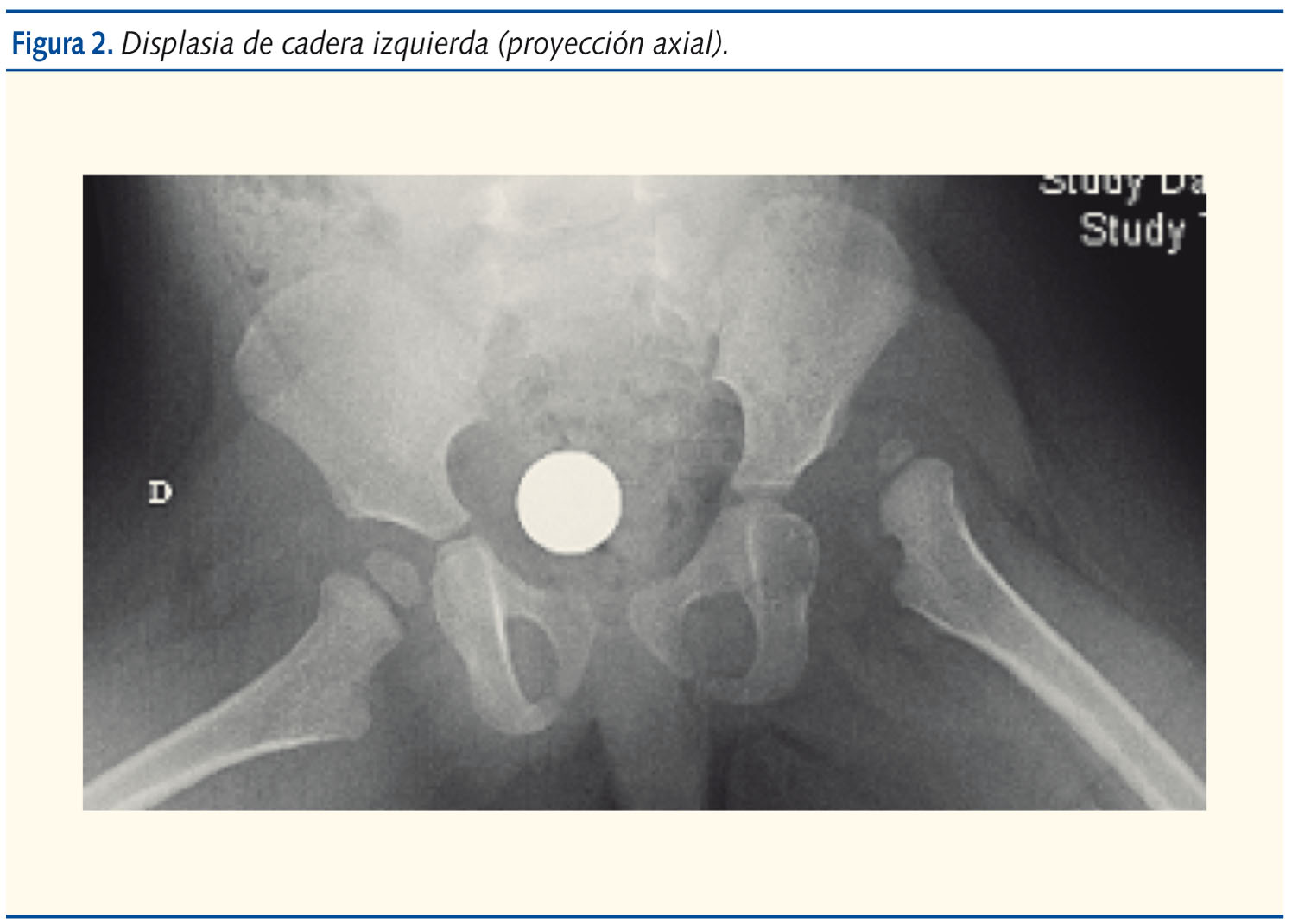
Comentario
Displasia evolutiva de cadera (DEC) es el término utilizado actualmente para designar una condición en la que la cabeza femoral tiene una relación anormal con el acetábulo. Comprende la luxación (completa o parcial), la inestabilidad o la luxabilidad, y también cambios radiológicos que reflejan una formación inadecuada del acetábulo. Se prefiere “evolutiva” a congénita porque los cambios no siempre son detectables al nacimiento, y “displasia” en vez de luxación porque se amplía el espectro de cambios que es posible encontrar en estos pacientes3.
La incidencia de DEC varía según los medios de detección, la edad del paciente y los criterios diagnósticos4. No existe un patrón oro definitivo. Aun así, se puede decir que se trata de la anomalía musculoesquelética más frecuente de la infancia. Se acepta de manera general que la presencia de inestabilidad o displasia de cadera clínicamente importantes afecta a 3-5 de cada 1000 nacidos vivos5.
La patogénesis es multifactorial: factores mecánicos (presentación podálica, oligohidramnios, primogénitos, etc); laxitud ligamentosa (inducida por las hormonas maternas que relajan el suelo pélvico); herencia6,7. Aunque se ha descrito la displasia acetabular primaria, actualmente se acepta que la displasia es consecuencia de la relación anormal entre el fémur y el acetábulo, y no su causa8.
Se han descrito varios factores de riesgo (FR). Los más importantes desde el punto de vista de los estudios y recomendaciones de cribado son: 1) presentación podálica; 2) sexo femenino, y 3) antecedentes familiares de DEC. También se ha descrito asociación con otras anomalías musculoesqueléticas: tortícolis congénito, metatarsus adductus, talipes equinovarus o calcaneovalgus, primogénito, entre otros6. Si bien es cierto que en niños que presentan estos FR la DEC es más frecuente, la realidad es que la mayoría de los pacientes con DEC no los presentan. Solo el 10-27% de los pacientes con DEC tienen FR6,9. Es decir, el típico paciente con DEC no presenta ninguno de estos factores de riesgo, salvo el sexo femenino (80%).
El tratamiento de la DEC es más sencillo y exitoso si se comienza de manera precoz (antes de los seis meses). Aunque la exploración de la cadera es la maniobra de evaluación musculoesquelética más frecuente el primer año de vida10, la prevalencia de casos tardíos se ha mantenido estable11. A primera vista, y dados los recursos disponibles para el clínico actualmente, esto nos resulta cuanto menos desconcertante, pero una revisión de la bibliografía reciente parece inclinar ostensiblemente la balanza hacia una política de cribado clínico universal y uso de la ecografía de forma selectiva.12-14
Existe evidencia a favor del cribado universal. Zenios et al. estudiaron el impacto de una política de cribado selectivo durante cinco años: no redujo la incidencia de casos de presentación tardía15. Existe también evidencia en contra. Dos de los consensos más importantes y extensos publicados no lo recomiendan. El primero, de la Asociación Americana de Pediatría, en el año 2000, recomienda ecografía a las seis semanas de vida solo en niñas con antecedentes familiares de displasia y en todos los nacidos en presentación podálica12. En Canadá, otra extensa revisión publicada en el año 2001 contempla la exploración clínica únicamente durante el primer año de vida en todos los niños y ecografía solo ante sospecha clínica, obviando realizarla en lactantes con FR13. La complejidad de los datos se refleja mejor aún en otra revisión, esta vez de los servicios preventivos estadounidenses. Estos concluyen que, aunque el cribado ecográfico universal permite detectar más tempranamente la DEC, la alta tasa de resolución espontánea y la mala calidad de la evidencia hacía imposible realizar recomendaciones definitivas a favor o en contra14. Mencionaremos también, por el importante tamaño de la muestra, un estudio prospectivo publicado en 2002 que incluyó 28 676 niños, de los que se aplicó cribado ecográfico selectivo a aquellos con FR o sospecha clínica: los resultados obtenidos pusieron de manifiesto la incapacidad del uso de la ecografía selectiva para disminuir la necesidad de cirugía con respecto a la exploración física aislada15.
Si se aplicase una política de cribado ecográfico universal en el periodo neonatal, y se tratase a todos aquellos con una cadera con alteraciones, no cabe duda de que se estaría sometiendo a un tratamiento innecesario a la mayoría de ellos, dado que la evolución natural de la mayor parte de estas alteraciones es hacia la resolución espontánea16-20. Las desventajas del tratamiento innecesario son múltiples; entre ellas, la necrosis avascular de la cabeza del fémur. Sin embargo, la frecuencia de esta complicación es directamente proporcional al tiempo que se tarde en instaurar el tratamiento. En los casos de displasia leve, la frecuencia de esta complicación está entre 0 y 1%21. En la inmensa mayoría son necrosis de grado I, siguen una evolución espontánea y no dejan secuelas22. No olvidemos tampoco los efectos psicológicos sobre los padres23 y las dificultades en la interacción madre-hijo en niños en tratamiento con arnés24. Además, el carácter evolutivo de la DEC determinará que niños con un cribado ecográfico negativo inicial desarrollen más adelante la enfermedad, por lo que ni aun así se evitan por completo los casos de presentación tardía subsidiarios de cirugía.
En algún punto entre estas dos propuestas tiene que existir la mejor solución, una que no consienta que sigan apareciendo casos que requieran tratamiento quirúrgico y con alto riesgo de secuelas funcionales, y que a la vez permita que los casos que van a evolucionar espontáneamente a la curación lo hagan sin que se sometan a un tratamiento innecesario no exento de complicaciones y efectos secundarios.
El seguimiento cuidadoso por profesionales experimentados en el diagnóstico y manejo de la DEC de los lactantes que en un primer estudio (hecho antes de las seis semanas) tengan signos ecográficos de displasia leve sería una opción que hasta ahora ya ha demostrado ser una estrategia segura en países como Alemania, Reino Unido y Eslovenia, dejando evolucionar a la curación espontánea a la mayoría y, a la vez, captando a ese pequeño grupo de los que se beneficiarán de un tratamiento precoz y que por otros medios (antecedentes y examen físico) pasarían inadvertidos. Esta estrategia ha demostrado a su vez disminuir la necesidad de resolución quirúrgica sin incrementar los costes sanitarios25-27.
No pretendemos dar una respuesta definitiva para un problema sobre el que existe tanta controversia y sobre el que se han pronunciado profesionales con gran experiencia. El cribado universal puede llevar a sobrediagnóstico y sobretratamiento, pero no necesariamente de forma ineludible. Una primera ecografía positiva podría indicar solo la necesidad de un seguimiento individualizado. Por otro lado, está demostrado que el cribado selectivo deja de detectar, aun en las mejores manos, a un contingente de niños que acaban requiriendo tratamientos más agresivos y con peor pronóstico funcional. No parece que exista una estrategia perfecta, pero nos cuesta trabajo conformarnos con la idea de que en la España de este siglo sigamos viendo niños con diagnóstico tardío y alto riesgo de padecer secuelas de por vida a causa de una patología fácil de prevenir. Podemos y debemos hacerlo mejor.
Bibliografía recomendada
- Aronsson DD, Goldberg MJ, Kling TF Jr, Roy DR. Developmental dysplasia of the hip. Pediatrics. 1994;94:201-8.
- Burger BJ, Burger JD, Bos CF, Obermann WR, Rozing PM. Neonatal screening and staggered early treatment for congenital dislocation or dysplasia of the hip. Lancet. 1990;336:1549-53.
- Klisic PJ. Congenital dislocation of the hip: a misleading term. Brief report. J Bone Joint Surg. 1989;71:136.
- Kocher MS. Ultrasonographic screening for developmental dysplasia of the hip: an epidemiologic analysis (part I). Am J Orthop. 2000;29:929-33.
- Bialik V, Bialik GM. Developmental dysplasia of the hip: a new approach to incidence. Pediatrics. 1999;103:93-9.
- Beaty JH. Congenital and developmental dysplasia of the hip. In: Canale ST, Beaty JH (eds.). Campbell’s Operative Orthopaedics. Philadelphia: Mosby; 2007. p. 1180-98.
- Hosalkar HS, Horn D, Friedman JE, Dormans JP. The Hip. In: Kliegman RM, Behrman RE, Jenson HB, Stanton BF (eds.). Nelson Textbook of Pediatrics. Philadelphia: Saunders; 2007. p. 2800-5.
- Harris WH. Etiology of osteoarthritis of the hip. Clin Orthop Relat Res. 1986;213:20-33.
- Mooney JF, Emans JB. Developmental dislocation of the hip: a clinical overview. Pediatr Rev. 1995;16:299-303.
- Azzopardi T, Van Essen P. Late diagnosis of developmental dysplasia of the hip: an analysis of risk factors. J Pediatr Orthop B. 2011;20:1-7.
- Mahan ST, Katz JN, Kim YJ. To screen or not to screen? A decision analysis of the utility of screening for developmental dysplasia of the hip. J Bone Joint Surg Am. 2009;91:1705-19.
- Lehman HP, Hinton R, Morello P. Developmental dysplasia of the hip practice guideline: technical report. Committee on Quality Improvement, and Subcommittee on Developmental Dysplasia of the Hip. Pediatrics. 2000;105:57.
- Patel H; Canadian Task Force on Preventive Health Care. Preventive health care, 2001 update: screening and management of developmental dysplasia of the hip in newborns. CMAJ. 2001;164:1669-77.
- Shipman SA, Helfand M, Moyer VA, Yawn BP. Screening for developmental dysplasia of the hip: a systematic literature review for the US Preventive Services Task Force. Pediatrics. 2006;117:557-76.
- Paton RW, Hossain S, Eccles K. Eight-year prospective targeted ultrasound screening program for instability and at-risk hip joints in developmental dysplasia of the hip. J Pediatr Orthop. 2002;22:338-41.
- Rabin DL, Barnett CR. Untreated congenital hip disease. A study of the epidemiology, natural history and social aspects of the disease in a Navajo population. Am J Public Health Nations Health. 1965;55:1-44.
- Weinstein SL. Natural history of congenital hip dislocation and hip dysplasia. Clin Orthop Relat Res. 1987;225:62-76.
- Gillam SJ, Foss M, Woolaway M. Late presentation of congenital dislocation of the hip: an audit. Br J Gen Pract. 1990;40:236-7.
- Riboni G, Bellini A, Serantoni S, Rognoni E, Bisanti L. Ultrasound screening for developmental dysplasia of the hip. Pediatr Radiol. 2003;33:475-81.
- Mahan ST, Katz JN, Kim YJ. To screen or not to screen? A decision analysis of the utility of screening for developmental dysplasia of the hip. J Bone Joint Surg Am. 2009;91:1705-19.
- Walton MJ, Isaacson Z, McMillan D, Hawkes R, Atherton WG. The success of management with the Pavlik harness for developmental dysplasia of the hip using a United Kingdom screening programme and ultrasound-guided supervision. J Bone Joint Surg Br. 2010;92:1013-6.
- Gardner F, Dezateux C, Elbourne D, Gray A, King A, Quinn A. Collaborative Hip Trial Group. The hip trial: psychosocial consequences for mothers of using ultrasound to manage infants with developmental hip dysplasia. Arch Dis Child Fetal Neonatal Ed. 2005;90:17-24.
- McHale KA, Corbett D. Parental noncompliance with Pavlik harness treatment of infantile hip problems. J Pediatr Orthop. 1989;9:649-52.
- Treiber M, Tomazic T, Tekauc-Golob A, Zolger J, Korpar B, Burja S et al. Ultrasound screening for developmental dysplasia of the hip in the newborn: a population-based study in the Maribor region, 1997-2005. Wien Klin Wochenschr. 2008;120:31-6.
- von Kries R, Ihme N, Oberle D, Lorani A, Stark R, Altenhofen L et al. Effect of ultrasound screening on the rate of first operative procedures for developmental hip dysplasia in Germany. Lancet. 2003;362:1883-7.
- Elbourne D, Dezateux C, Arthur R, Clarke NM, Gray A, King A et al. UK Collaborative Hip Trial Group. Ultrasonography in the diagnosis and management of developmental hip dysplasia (UK Hip Trial): clinical and economic results of a multicentre randomised controlled trial. Lancet. 2002;360:2009-17.
- Gray A, Elbourne D, Dezateux C, King A, Quinn A, Gardner F. Economic evaluation of ultrasonography in the diagnosis and management of developmental hip dysplasia in the United Kingdom and Ireland. J Bone Joint Surg Am. 2005;87:2472-9.
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.




